タンパク質発現、ハイスループットスクリーニング、遺伝子改変など、ウイルスによる遺伝子導入の最終目標が何であっても、ウイルス力価を丁寧に測定することで、遺伝子導入の成功率は上がります。遺伝子導入効率(例:細胞に侵入するウイルスの数)や、感染細胞の染色体に組み込まれる目的遺伝子のコピー数を決定する上で、あらかじめウイルス溶液のウイルス粒子数や感染単位を知ることは重要です。本ブログでは、上手に実験をスタートしていただくため、レンチウイルス力価測定に関して、様々な測定法や各方法にどのような相関性があるのかをご紹介いたします。
・レンチウイルス作製の基礎と力価測定
レンチウイルスの力価測定には、主に2つの方法があります。1つは、ウイルスゲノムまたはウイルスタンパク質の量を測定してウイルス粒子濃度を測定する物理的な方法であり、もう1つは、遺伝子導入能を有する粒子数(IFU/mL)を測定する機能的(生物的)な方法です。これらの方法で何を測定するのかを理解するため、まずは、レンチウイルス作製ワークフロー(図1)を参考に、一般的なウイルス調製プロセスで何が産生されるのかを確認してみましょう。
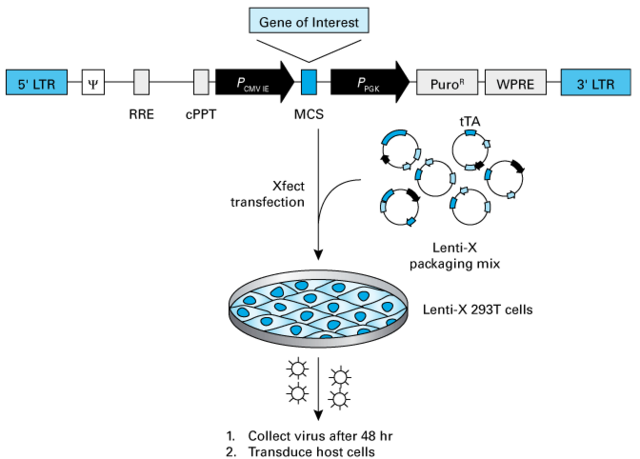
組換えレンチウイルスの機能に必要なすべてのシスエレメント配列を含んだバックボーンプラスミド(トランスファーベクター)に標的配列をクローニングします(図1A)。次に、トランスファーベクターと、ウイルス粒子の産生に必要なすべてのウイルスタンパク質を発現するプラスミドベースのパッケージングミックスを混合します。その後、トランスフェクション試薬(リポソームや合成ポリマー)を用いてトランスファーベクターとパッケージングミックスを、ウイルス産生用細胞(主に293T細胞)に導入します。
組換えレンチウイルスの機能に必要なすべてのシスエレメント配列を含んだバックボーンプラスミド(トランスファーベクター)に標的配列をクローニングします(図1A)。次に、トランスファーベクターと、ウイルス粒子の産生に必要なすべてのウイルスタンパク質を発現するプラスミドベースのパッケージングミックスを混合します。その後、トランスフェクション試薬(リポソームや合成ポリマー)を用いてトランスファーベクターとパッケージングミックスを、ウイルス産生用細胞(主に293T細胞)に導入します。
| ベクターに必要な配列 | 役割 |
|---|---|
|
ロングターミナルリピート (LTR)
|
レトロウイルスDNAの宿主染色体への挿入を媒介する。 |
|
レンチウイルスパッケージングシグナル (Ψ)
|
ウイルスゲノムのカプシドへのパッケージングを制御する。 |
|
Rev応答エレメント (RRE)
|
スプライシングされていないウイルスゲノムRNAの核外輸送を促進することでウイルス産生量を上げる。 |
|
セントラルポリプリン配列/セントラルターミネーション配列 (cPPT)
|
標的細胞感染時にウイルスゲノムの核内取り込みを増加させる「DNAフラップ」を形成する。cPPT/CTSエレメントはベクターの宿主ゲノムへの挿入と遺伝子導入効率を向上させる。 |
|
ウッドチャック肝炎ウイルス転写後制御因子 (WPRE)
|
ポリA付加シグナルのリードスルーを防ぎ、RNAのプロセシングと成熟を促進し、RNAの核外輸送を増加させる。パッケージング細胞内のウイルスゲノム転写物に作用してベクターパッケージングを促進し、ウイルス力価を増大させる。遺伝子導入された標的細胞では、WPREはmRNA転写物の成熟を促進することにより、導入遺伝子の発現を増加させる。 |
図1. レンチウイルス作製ワークフローの例 A:クロンテック社の第4世代レンチウイルスパッケージングシステムのワークフロー B:クロンテック社レンチウイルスベクターのシスエレメント。エレメントは、HIV-1ウイルス由来。
その結果、ウイルス粒子が上清に放出されます。この上清中(図2)には、感染性を有する完全な粒子、非感染性粒子、空のカプシド構造タンパク質(例:p24)が含まれます。物理的な力価測定法
(qRT-PCR法、p24 ELISA法、Lenti-X GoStix Plus)は、比較的シンプルに実施することができますが、機能性ウイルス粒子と非機能性ウイルス粒子の両方をカウントしてしまいます(直接または間接的に上清に放出されたウイルス成分を分析するためです)。一方、機能的な力価測定法では、標的細胞に遺伝子導入可能なウイルス粒子(例:感染単位又はIFU)を特異的に定量化しますが、時間がかかり、操作も多くなります。
(qRT-PCR法、p24 ELISA法、Lenti-X GoStix Plus)は、比較的シンプルに実施することができますが、機能性ウイルス粒子と非機能性ウイルス粒子の両方をカウントしてしまいます(直接または間接的に上清に放出されたウイルス成分を分析するためです)。一方、機能的な力価測定法では、標的細胞に遺伝子導入可能なウイルス粒子(例:感染単位又はIFU)を特異的に定量化しますが、時間がかかり、操作も多くなります。
図2. 力価測定法の種類 A:レンチウイルスパッケージング上清に存在する産物。物理的な測定法では、機能性ウイルス粒子や非機能性ウイルス粒子だけではなく、上清に放出された空のカプシド構造タンパク質
(例:p24)も測定される。機能的な力価測定法は、機能性ウイルス粒子を特異的に測定する。B:標準的な力価測定法のタイムライン。Lenti-X GoStix Plus:上清中のレンチウイルスp24を検出するラテラルフロー型の測定法。qRT-PCR法:ウイルスRNAゲノムをqRT-PCRで定量化する方法。ELISA法:カプシド構造タンパク質p24の量を測定する方法。qPCR法:細胞染色体に挿入されたDNAプロウイルスを
qPCRで検出する方法。IFU(FACS)法:RFP/GFP陽性細胞のFACS解析によって感染細胞率を測定する方法。IFU(薬剤選択)法:遺伝子導入細胞集団における薬剤耐性コロニー数を定量化して感染単位を測定する方法。
(例:p24)も測定される。機能的な力価測定法は、機能性ウイルス粒子を特異的に測定する。B:標準的な力価測定法のタイムライン。Lenti-X GoStix Plus:上清中のレンチウイルスp24を検出するラテラルフロー型の測定法。qRT-PCR法:ウイルスRNAゲノムをqRT-PCRで定量化する方法。ELISA法:カプシド構造タンパク質p24の量を測定する方法。qPCR法:細胞染色体に挿入されたDNAプロウイルスを
qPCRで検出する方法。IFU(FACS)法:RFP/GFP陽性細胞のFACS解析によって感染細胞率を測定する方法。IFU(薬剤選択)法:遺伝子導入細胞集団における薬剤耐性コロニー数を定量化して感染単位を測定する方法。






 natsukac
natsukac

